Telemedicinlösningen ViPHS skulle kunna utgöra ett viktigt tillskott till strokevården och bidra till att träffsäkert identifiera, triagera och transportera rätt patienter snabbare till trombektomi. Problemet är att det trots ett uttalat kliniskt behov inte används – nyttiggörandet och spridningen går trögt. Här diskuteras möjliga orsaker och lösningar för att ändra på detta.
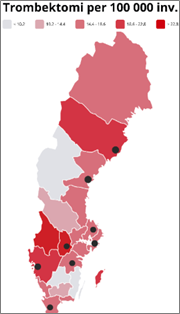
Stroke är en av våra vanligaste sjukdomar och avgörande för vårdutfallet är tiden till behandling. Majoriteten (85%) är ischemisk stroke där reperfusionsbehandling med trombolys (IVT) eller trombektomi (EVT) är alternativen. För patienter med storkärlsocklusion har EVT visat sig vara en fördelaktig metod – en ”tumregel” skattar att en timmas tidsbesparing ger dubblerad behandlingseffekt. IVT erbjuds idag på alla akutsjukhus (72) medan EVT enbart på ett begränsat antal (8), ojämnt fördelade över landet (figur 1).
I ett glesbefolkat land som Sverige med stora avstånd innebär det stora utmaningar att erbjuda bästa möjliga vård oavsett var man bor – tiden till ”rätt” behandling och sjukhus måste göras kortast möjlig. Förhållandena idag tydliggörs i EVAS (Registret för endovaskulärbehandling av stroke) årsredovisning 2024: ”Detta understryker att förbättringen framåt inte främst handlar om proceduren i sig, utan om hur snabbt och träffsäkert vi identifierar, triagerar och transporterar rätt patienter i rätt tid.”
Majoriteten av patienter har sin första vårdkontakt med ambulanssjukvården. Följaktligen blir besluten här avgörande för hur snabbt optimal behandling kan erbjudas. Särskilt viktigt blir det att med god precision identifiera de patienter som med hög sannolikhet är aktuella för EVT och där direkttransport till EVT sjukhus är lämplig och möjlig; vård- och tidsmässigt samt logistiskt.
Telemedicin rekommenderades
ViPHS utformades i ett tvärvetenskapligt projekt med start 2015 och med mål att via telemedicin stödja prehospitala beslut om destination och behandlingsstrategi inom och mellan regioner. Telemedicin som rekommendation för den prehospitala vården har även funnits i de nationella riktlinjerna för stroke sedan 2020.
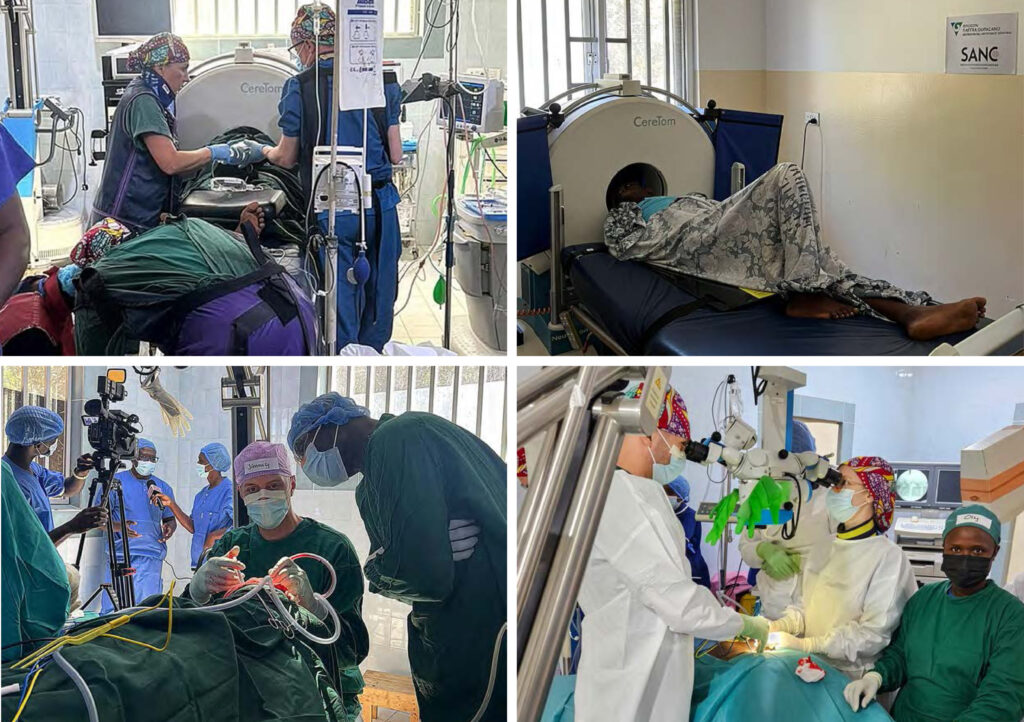
ViPHS är ”klassisk” telemedicin, liknande den som introducerades för hjärtinfarkt på 1990 talet genom MobiMed – där artikelförfattaren var en av de drivande. I MobiMed var EKG grunden för bedömning men något liknande lämpligt i ambulans finns tyvärr inte för stroke. I ViPHS har då etablerade och kliniskt rekommenderade NIHSS (National Institute of Health Stroke Scale), med hög specificitet men inte så god sensitivitet, valts för att identifiera EVT kandidater. Detta innebär att de som identifieras är sannolika – men ett antal kan missas. Att genomföra NIHSS kräver en strokeläkare, och via video med tre kameror samt ljudöverföring tillgängliggörs denna kompetens i ambulansen (figur 2). ViPHS beskrivs detaljerat i flera artiklar (referenslista) och bygger på fyra komponenter:
- Validerad metod för bedömning av LVO-risk; NIHSS
- Rutin och krav för genomförande av NIHSS via telemedicin
- Tekniklösning för att möjliggöra NIHSS skattning på distans
- Anpassad prehospital vårdrutin/vårdprocess

Vid användning av ViPHS i 15 ambulanser upplevde ambulanspersonal och strokekonsulter stora fördelar med videokonsultationer i stället för telefonsamtal. Pilotprojekten pågick i ett år i VGR och Södra Älvsborg.
ViPHS idag – och framöver
ViPHS är idag metodologiskt testad, tekniskt relativt okomplicerad, kostnadseffektiv och skalbar samt kan användas i stor skala i alla ambulanser och av reguljära besättningar i samverkan med sjukhusets strokeexpertis för att öka precisionen i de prehospitala besluten. ViPHS testades operativt med goda resultat redan 2019/2020 och har under en 10-årsperiod redovisats och presenterats i vad som kan anses vara ”rätt” kanaler och till ”rätt” aktörer inom akademi, sjukvård och näringsliv. I tillägg upplät initiativtagarna tillgängliga projektresultat till VGR 2019/2020 för att möjliggöra en regionalt ledd, vid tidpunkten, förmodad snabb implementering och referens – ett arbete som i inledningen av 2026 ännu pågår.
Trots en accepterad välkänd problembild (bl.a. EVAS) och tillgång till en demonstrerad och kommunicerad vårdmodell har vidare aktiviteter, spridning och nyttiggörande inom och mellan regioner inte tagit fart. Borde inte ViPHS, och så som det uttryckts från olika håll, vara en självklarhet, en ”no brainer” till ett bredare införande utifrån aktuell klinisk utmaning?
Tyvärr är ViPHS här inte en unik företeelse. Det finns många projekt inom exempelvis gräns- och verksamhetsöverskridande telemedicin som i slutändan fallerat, dött och hamnat i gruppen ”Tekniken, och kliniska nyttan, var inte problemet – det var annat!”. Alltså själva nyttiggörandet av innovationsidén, uteblir – de blir ”nyårsraketer” som en kort stund lyser upp himlen och ger hopp, men sedan försvinner. I ViPHS fallet skulle detta ”annat” kunna vara:
- Dålig ”marknadsföring” från projektgruppen.
- Felaktigt vald modell mot bredare nyttiggörande efter de inledande operativa testerna. Kanske skulle projektgruppen redan 2019/2020 ännu mer aktivt själva inlett arbete med att sprida ViPHS mot sjukvård och företag, eller startat ”eget”.
- Att den kliniska nyttan, värdet och relevansen missbedömts/misstolkats. Saknas det tillräckligt kliniskt ”sug”, vilja eller intresse för att faktiskt förändra vårdmodeller för att hantera vad som beskrivs av EVAS?
- Att ViPHS inte är tillräckligt ”flashigt”, för ”jordnära”, och idag innehåller för lite AI inslag i tidens anda för att ge avtryck i ”informationsbruset”.
- Att det krävs/saknas lokalt drivande entreprenöriella eldsjälar med ork, mod, vilja och kraft, samt möjligt framtida anseende och uppskattning, att driva och samordna lokal och regional förankring samt införande.
- Att affärsmodellen inte är självklar och/eller att införsäljningen är pionjärliknande, komplicerad och riskerar att bli utdragen vilket gör de naturliga företag som kontaktats tveksamma, ointresserade eller avvisande – trots att befintligt kunderbjudande stärks.
- Att de flesta innovationsidéer, som ViPHS, normalt inte kan leda till nya företag för att bli innovationer – vägen måste gå via de etablerade. Saknas då nödvändiga dubbelriktade vägar, incitament, förtroende och genuint intresse att samspela med t.ex. akademien?
Har nytta visats?
ViPHS har testats i fullskaliga simuleringar och två operativa piloter och bygger på ett ”videotillägg” till en vårdrutin som infördes redan 2016 i VGR. Denna rutin styr konsultation mellan ambulans- och strokeläkare via telefon. ViPHS är alltså en videoförstärkt telefonkonsultation. Den första pilotinstallationen pågick i 12 månader med tre ambulanser i Södra Älvsborg och resultat har redovisats på konferenser och artikel. Den andra piloten, ledd av VGR, pågick också i 12 månader och där ingick 12 ambulanser spridda i regionen. Vid användning upplevde ambulanspersonal och strokekonsulter stora fördelar med videokonsultationer i stället för telefonsamtal.
Det kan tyckas att ViPHS, trots ovanstående, inte är tillräckligt utvärderat med avseende på exempelvis patientnytta, hur många patienter som berörs eller hur mycket tid som faktiskt kan sparas. Naturligtvis hade det varit önskvärt med mer omfattande operativ erfarenhet. Men för ViPHS, liksom MobiMed på sin tid, där tekniken är en möjliggörare utformad utifrån aktuellt kliniskt kunskapsläge, delas utmaningen att ”nyttoforskning” endast kan bedrivas när ”verktyget” faktiskt finns på plats, och i tillräcklig omfattning.
Antalet möjliga patienter är numeriskt stort men de är spridda över stora geografiska områden. Därför krävs ett stort antal ambulanser för att uppnå patienttal som möjliggör jämförande studier. Beräkningar indikerar att det skulle krävas flera hundra patienter (kontroll och intervention) för att kunna påvisa statistisk signifikans för frågan ”utfall med eller utan”. För att erhålla ett sådant material på ”rimlig” tid kommer en testinstallation i princip att motsvara ett större införande – ekonomiskt och organisatoriskt. Därför är det rimligt, och närmast nödvändigt, att beslut fattas på premisser som lyckade simuleringar och piloter samt kända fakta som vikten av snabbare och effektivare vårdkedjor, effekten av vårdval/behandlingar och de något odefinierade argumenten ”klinisk känsla och insikt” eller ”magkänsla”.
Hur många och vad blir tidsvinsten per krona
I ViPHS har tidsvinst definierats som summan av DIDO tid (Door In Door Out) på första sjukhus vid vidaretransport tillsammans med den extra transporttid detta kan innebära. Internationella studier visar att DIDO kan skattas till cirka 1,5 timma. I beräkningar med VGR som mall hamnar tilläggstid runt 0 – 1,5 timmar. Totalt alltså en fördröjning på 1–3 timmar.
ViPHS är en kostnadseffektiv och lätt skalbar lösning. Videokomponenterna till en ambulansinstallation motsvarande den som användes i simuleringar och pilot 1 kostar idag cirka 20,000 SEK (exkl. moms) per ambulans. Till detta tillkommer fysisk installation, mobil router (ofta på plats) samt smartphone eller tablet. På sjukhussidan behövs smartphone med videoapp. I de inledande testerna användes en gratis app för video men denna del kan utformas på olika sätt utifrån regionala önskemål och policys.
Skattning för antal konsultationer och patienter har gjorts för ett geografiskt område i VGR med cirka 1,700 fall per år och ett 70-tal ambulanser. Resultatet blev 150–200 konsultationer per år, motsvarande 2–4 per ambulans. I pilot 2 ingick 12 ambulanser och det förväntades då cirka 25 konsultationer. Resultat indikerar ett 20-tal, vilket verkar rimligt då i praktiken aldrig alla ambulanser var tillgängliga 365/24/7. I efterhand har journalgranskning bekräftat att ambulansen inte missade några konsultationsfall. På Sahlgrenska gjordes 2024 cirka 370 trombektomier varav runt 50% var sekundärtransport från annat sjukhus. Med antagandet att 50% kunnat identifieras prehospitalt blir resultatet runt 90 direkttransporter.
Har dålig ”marknadsföring” varit ett skäl till att uppskalning och bredare nyttiggörande uteblivit. Detta är vanskligt att besvara, men bilden är att en hel del ansträngningar gjorts för att nå ut till ”rätt” aktörer inom sjukvård, akademi och näringsliv. Även intresseorganisationer och media har adresserats såväl direkt som via sociala media och pressreleaser.
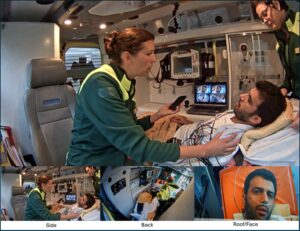
Figur 2. ViPHS i ambulansen samt
de 3 videobilderna. Bilder från simulering med skådespelare som patient.
Summering
Trots all positivism är känslan att komplexiteten i att hantera och praktiskt driva och genomföra införande hämmar nyttiggörande av regionalt och tvärregionalt kraftfulla och ganska självklara telemedicinlösningar som ViPHS – och som för MobiMed på 1990-talet. För de som sikar på införande gäller initialt att ”sälja in” konceptet till alla berörda, sedan hantera finansiering, fördela kostnader samt avgöra vem eller vilka som organisatoriskt skall leda arbetet. Om man väljer att inte upphandla lösningen tillkommer att i egen regi även hantera installation, drift, support samt ”produktvård”, förvaltning och underhåll. Utmaningen är hämmande och kan överskugga dialogen runt vikten och betydelsen av den faktiska nytta som kan levereras till patienter. Hur sjukvården bäst skall hantera situationen är en viktig fråga att adressera då annars potentiellt värdefulla vårdinnovationer riskerar att utebli.
För att stötta och bidra till bredare nyttiggörande finns en gedigen kunskapsmassa, dokumentation och kompetens att tillgå som inkluderar kliniska motiv och överväganden, regulatoriska frågor, kalkyler, utvärderingar, teknik samt marknadsaspekter. Initiativtagarna vill se, och medverka till, vidare spridning och artikelförfattaren är en ingång för de som vill hjälpa till. Tvärdisciplinär och organisatorisk samverkan krävs för att ViPHS ska nå verklig innovation och bli en ”no brainer” till nytta för många patienter.
Text: Bengt Arne Sjöqvist
I samarbete med:
Magnus Andersson Hagiwara Professor, Högskolan i Borås
Annika Nordanstig Överläkare neurologi, Sahlgrenska Universitetssjukhuset
Referenser i urval
Sjöqvist B A et al. Telemedicine utilizing video streaming in prehospital assessment of stroke – an opportunity to shorten time to thrombectomy. Health and Technology, (2025) 25:126, doi.org/10.1007/s12553-025-00981-9
Fullständig referenslista tillgänglig här: https://drive.google.com/file/d/1c4dSo7rtauSYn88gY2UMwTEBnmd0UHXQ/view?usp=drive_link