En karta till hjärnans utveckling och dess inflammation
Att förstå hur hjärnan utvecklas och hur den reagerar vid sjukdom kräver att man undersöker fler än en biologisk dimension. Det kräver ett utforskande på en flerdimensionellnivå, vilket innebär att noggrant studera tre av kroppens grundläggande byggstenar: DNA, RNA och proteiner, ur både tidsmässigt och rymdssmässigt perspektiv. Här skriver Tony Jimenez-Beristain om sin forskning.
Denna tredimensionella utmaning har antagits av forskargrupper ledda av professor Gonçalo Castelo-Branco och doktor Leslie Rubio Rodríguez-Kirby vid Karolinska Institutet samt professor Rong Fan och doktor Di Zhang vid Yale University, USA, bland andra medarbetare i en aktuell studie som nyligen publicerades i den ledande vetenskapliga skriften Nature. Resultatet är en detaljerad karta över mushjärnan under utveckling från postnatalperioden till ung ålder (typisk 3-4 veckors ålder) i olika delar av hjärnan, både under fysiologiska förhållanden och inflammatoriska tillstånd.

Konstnärlig visualisering av hjärnans föränderliga struktur i flera dimensioner, inspirerad av La persistencia de la memoria. Illustration: AMAGOIA AGIRRE, KAROLINSKA INSTITUTET
Studien bygger på en avancerad multi-omik (från det grekiska ordet ome som betyder helhet) teknologi kallad DBiT (Deterministic Barcoding in Tissue). Denna teknik uppfanns av professor Rong Fans team och vidareutvecklades i samarbete med professor Gonçalo Castelo-Branco. I korthet innebär DBiT:s teknologi små DNA-fragment märkta med unika streckkoder som infunderas på histologiska vävnadssnitt, likadant som att använda GPS för att kartlägga en stad, men istället för gator och byggnader DBiT kartlägger molekyler såsom DNA (kromatin), RNA och proteiner märkta med de unika DNA-streckkoderna som senare avkodas för att veta exakt var i vävnadensnitt varje informationsbit kommer ifrån, så varje molekyl har en lokation på ett rumsligt sammanhang.
Beständighet och minne
Kromatinåtkomst är en cellulär mekanism som gör att cellerna kan förbereda sig för att agera vid snabba förändringar, inkluderande sjukdom. Detta genom att göra sitt kromatin mer ”öppet”. tillgängligt för genuttryck (transkription), så celler snabbt kan reagera när rätt signal kommer eller när till exempel drastiska sjukdomsförändringar äger rum. För att få insikt i den utvecklande hjärnas genuttryck (RNA) och kromatinåtkomst profiler, designades en avancerad datormodelleringsprocess för att undersöka hur dem förändras över fem olika dimensioner: rymd = till exempel, hjärnans kortikala lager, tid = från födseln till tre veckors ålder och molekylärt = RNA/DNA/protein. Genom att integrera alla dessa dimensioner tillsammans upptäcktes flera distinkta mönster, som vart och ett visar hur gener uttrycks under hjärnans utveckling efter födseln. Flera gener som uttrycktes vid födseln, paradoxalt nog, antingen minskad i aktivitet över tid eller var helt frånvarande några veckor efter födseln. I kontrast kvarstod kromatinåtkomsten för vissa av dessa gener oberoende av tiden, vilket tyder på en sorts genetisk beständighet och minne av tidiga utvecklingsstadier. Det troligtvis möjliggör snabb respons och flexibilitet inför framtida förändringar, även efter att det grundläggande utvecklingsprogrammet inte längre är biologiskt nödvändig och har stängts av.
Myelin i olika faser
Axonogenes är en utvecklingsprocess där neurons axoner växer ut mot andra neuroner eller målorgan. Detta steg är avgörande för att bygga effektiva och funktionella nervkretsar. En fängslande observation var det tid och rymds överlappande koordinering i mognandet av corticofugal projektionsneuroner och myelinering. Myelinering är en process där oligodendrocyter lindar in neurons axoner i ett fettlager (det vill säga myelinlager), detta lager fungerar som en mycket effektiv isolering som bidrar till att kommunikation mellan neuroner färdas blixtsnabbt. Den här samordningen har funktionella anledningar, eftersom det här är en typ av neuroner som är kända för att skicka sina långa axoner till andra hjärnregioner och ryggmärgen. Kort förklarat, när kortikala neuroner mognar under olika utvecklingsstadier initierar yttre signaler förberedelsen av myelinbildning. Enligt våra resultat myeliniseras axoner först i cortex lager V och VI, följt av lager II och III. I corpus callosum gjordes en mycket spännande observation, myelinisering sker där på ett tids- och rumskoordinerat tvåvägsmönster: ett som startar lateralt och ett som startar centralt i corpus callosum för att sen fullborda en fullständing myelinering av hela corpus callosum. Denna åtkomst till gener som är viktiga för myelinproduktion i corpus callosum redan förberedd före den aktiva myeliniseringen behövde ske under hjärnutvecklingen, vilken kan tolkas som en form av cellberedskap. Både hjärnregioner, cortex och corpus callosum är centrala i studien eftersom båda genomgår patologiska förändringar vid multipel skleros, en sjukdom som står i fokus för professor Castelo-Brancos grupps forskning.
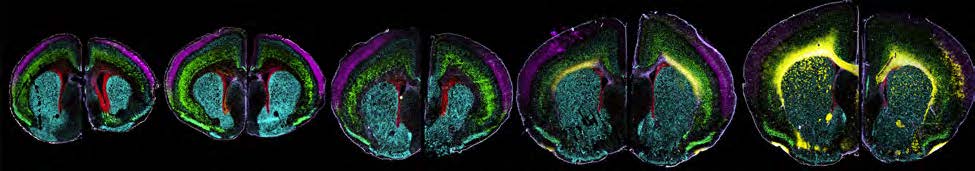
Avancerad kartläggning av den växande mushjärnan när myeliniseringen startar. Bilderna, tagna med CODEX teknik, visar utvecklingen från födseln (dag 0, vänster) till tre veckors ålder (dag 21, höger).
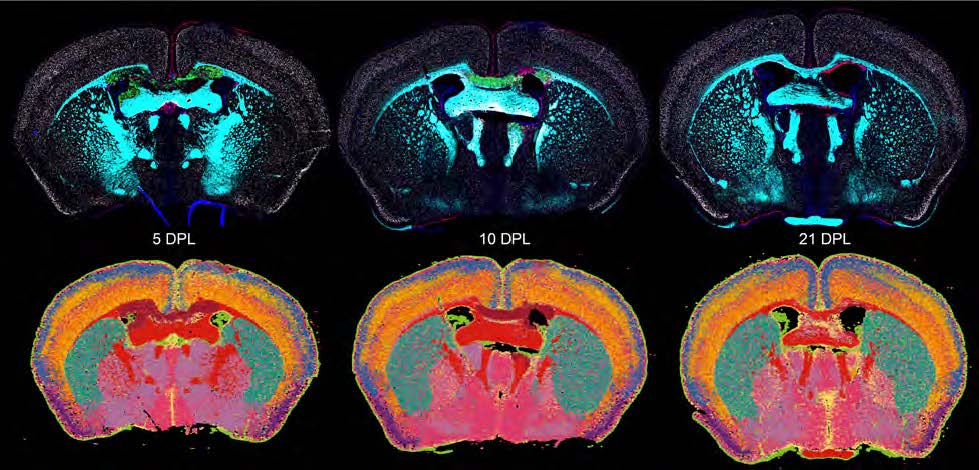
(Övre panel) Bilder av mushjärna som visar hur en experimentell skada utvecklas 5 och 10 dagar efter att den uppstått, samt hur vävnaden börjar läka efter 21 dagar. (Nedre panel) Samma område analyserat efter vilka proteiner som uttrycks, där olika celltyper grupperats och färgkodats utifrån sina egenskaper.
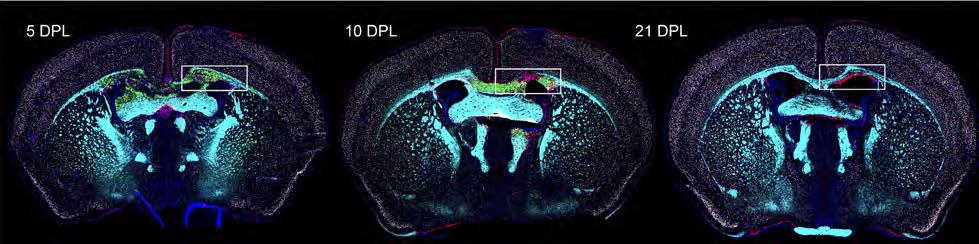
Bilder av mushjärna som visar hur en experimentell demyeliniserande skada utvecklas över tid – från tidig fas till påbörjad läkning efter tre veckor.
En omväg till inflammation
Professor Castelo-Brancos team har lång erfarenhet av prekliniska modeller för multipel skleros, bland annat en modell som kallas lysolecitin-inducerad demyelinisering, vilken användes i studien. Lysolecitin är en liten molekyl som oftas används som emulgerinsmedel. När det administreras direkt in i hjärnan skadas myelinet runt axonerna och en inflammatorisk reaktion uppstår, och därmed efterliknar denna behandling vissa patologiska aspekter av multipel skleros. När inflammation inducerades i den vuxen hjärnan via lysolecitin behandling kunde vi noggrant följa med upplösning på enskild cellnivå den morfologiska utvecklingen av skadan under flera dagar efter lysolecitinbehandlingen och även visualisera skadeåterhämtning via remyelinering. Som väntat detekterades CD45+-immunceller i centrum och närmsta omgivningen av skadan, samt i hjärnhinnan. Förvånande var att utöver CD45+ celler detekterades också CD11c+ mikrogliaceller relativt lång borta från centrum av skadan. CD11c+ mikroglia är en subtyp av mikroglia med en betydande roll under inflammation och det tros att de kan bidra till att rensa bort cell- och myelinrester och på så sätt stödja remyelineringen. Dessa fynd belyser att inflammation som härrör från en skada i en region av hjärnan kan sprida sig och leda till aktivering och mobilisering av skadereparerande mikroglia och immunceller även på långt avstånd (i distala platser) i hjärnan.
Varför denna studie spelar roll?
- Studien möjliggör skapandet av rumsliga, flerskiktade hjärnkartor på bevarad vävnad vilken låter studera vävnadens struktur i sitt ursprungliga sammanhang, celler, extracellulär matrix och arkitektur.
- Det öppnar för ett brett spektrum av tillämpningar, som till exempel diagnostik. Detta är avgörande för att förstå sjukdomsmekanismer, till exempel hur inflammation eller degeneration påverkar olika celltyper.
- Detta arbete ger en rik resurs för att utforska hur hjärnan utvecklas och anpassar sig till biologiska behov och drastiska ändringar, och erbjuder ledtrådar för att förstå neurologiska sjukdomar och utveckla nya behandlingar.
Läs mer:
Spatial dynamics of brain development and neuroinflammation. Di Zhang, Leslie A Rubio Rodríguez-Kirby, Yingxin Lin, Wenqi Wang, Mengyi Song, Li Wang, Lijun Wang, Shigeaki Kanatani, Tony Jimenez-Beristain, Yonglong Dang, Mei Zhong, Petra Kukanja, Shuozhen Bao, Shaohui Wang, Xinyi Lisa Chen, Fu Gao, Dejiang Wang, Hang Xu, Cong Ma, Xing Lou, Yang Liu, Jinmiao Chen, Nenad Sestan, Per Uhlén, Arnold Kriegstein, Hongyu Zhao, Gonçalo Castelo-Branco, Rong Fan, Nature, online 5 november 2025, doi: 10.1038/s41586-025-09663-y.