En enda tår från ögat kan innehålla samma information som en smärtsam och tidsödande lumbalpunktion – men helt utan risker. Det menar oftamologen Marlies Gijs.
– Den centrala frågan är förstås hur vi kan få ett kliniskt värde och faktiskt fastställa diagnos, säger hon.
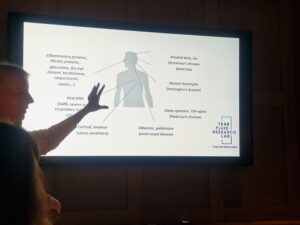
En tår innehåller flera hundra substanser och kan jämföras med blod när det kommer till att analysera en människas hälsotillstånd, visar Marlies Gijs forskning. Med hjälp av en liten bit papper sugs tårvätskan upp. I den finns information och biomarkörer, inte bara för ögonsjukdomar och inflammation, utan om hela kroppen och hjärnans tillstånd. Gijs menar att genom att analysera molekylerna syns flera hundra biomarkörer.
– Jag har i min forskning kunnat visa hur vi i tårvätskan kan se om en patient har Parkinsons, Alzheimers eller Huntington.

”Nu försöker vi visa att vi kan diagnostisera Alzheimers sjukdom med samma precision som med en invasiv lumbalpunktion. Om vi kan undvika ens ett fåtal sådana ingrepp är det en framgång”, säger Marlies Gijs. Foto: MEREL TUK
Det låter som att det går att se mer i en tår, än vad vi än så länge kan se i blod?
– Ja, för till exempel Alzheimers är lumbalpunktion den vanliga vägen för att fastställa diagnos. Att samla in tårar är i det sammanhanget betydligt mer skonsamt, säger Marlies Gijs.
Neurologi i Sverige träffar Marlies Gijs under en pressresa i Nederländerna mitt i kalla vintern 2026. Inte på flera år har snön legat kvar på gatorna i Maastricht och alla i gruppen skojar om att svenska reportern tagit med sig vintern på resan hit. Resan är arrangerad av det holländska turistrådet och Marlies Gijs var inbjuden en middag för att berätta om sin forskning och vi får tillfälle att sitta tillsammans.
det visar sig att Marlies Gijs bor i Dessel i Belgien och reser in till sitt jobb som forskare på ögonkliniken på Maastricht UMC. För henne var en akademisk karriär ingen självklarhet, men familjens plantskola ville hon inte engagera sig i. Istället började hon studera farmaci i Leuven. Med åren blev Gijs alltmer fascinerad av biokemi och intresserade sig för celler och molekyler. För drygt tio år sedan disputerade hon i Liège med inriktning på cancerforskning och har nu en forskartjänst inom biokemi och bitechnologi på Maastrich universitetssjukhus.
Covid i ögat
Sedan ett par år tillbaka har Marlies Gijs har all fokus på den vätska vi människor har i ögat och vad den kan säga om individen. Människan producerar cirka en till två mikroliter tårvätska per minut. Vätskan produceras och dräneras i ett slutet system som bidrar till att upprätthålla ögats hälsa. Gijs förklarar att allt som finns i luftburna partiklar hamnar på ögats yta, inklusive virus. Dessa måste snabbt brytas ned och sköljas bort. I början av covid-19-pandemin cirkulerade rykten i Kina om att viruset tog sig in i kroppen via ögonen.
– Vi började omedelbart undersöka detta. Vi kunde påvisa virus i tårvätskan, men hypotesen att detta var en huvudsaklig smittväg visade sig vara en myt, men jag förstod då att sjukdomen skulle gå att diagnosticera i ögat.
Den första artikeln, som kom 2021, om studien som visade att det var möjligt att detektera Alzheimers sjukdom i tårvätska bevisade inte att själen är ögats spegel, men väl hjärnans. Ögonen är embryologiskt sett utskott från hjärnan och kan därför spegla cerebrala sjukdomsprocesser. I tårvätskan uppmättes två av de viktigaste biomarkörer vi idag känner till om alzheimers, amyloid och tau. I studien hade tårvätska samlats in från totalt 65 individer, varav 23 patienter med subjektiv kognitiv svikt, 22 patienter med mild kognitiv störning, 11 patienter med demens samt 9 friska kontroller.
Marlies Gijs fortsätter att gräva djupare i vad en tår kan avslöja om kroppens tillstånd.
Nivåer av amyloid beta peptider, AB38, AB40 och AB42, samt total tau och fosforylerad tau, analyserades med multiplexa immunoassays. Nivåerna av AB40 och total tau var detekterbara i majoriteten av tårvätskeproverna, över 94 procent. Cerebrospinalvätska fanns tillgänglig från en undergrupp av patienterna. I denna grupp var nivåerna av total tau i tårvätska signifikant högre hos personer med demens jämfört med patienter med subjektiv kognitiv svikt.
Nivåerna av total tau i tårvätska var förhöjda hos patienter med neurodegeneration, klassificerad enligt A T N systemet, jämfört med patienter utan tecken på neurodegeneration. Negativa korrelationer observerades mellan AB42 i cerebrospinalvätska och total tau i cerebrospinalvätska, samt mellan AB42 i cerebrospinalvätska och total tau i tårvätska.
Sammanfattningsvis visade studien att tauproteiner i tårvätska har potential att vara associerade med sjukdomens svårighetsgrad och graden av neurodegeneration.
Sedan första publicering om tårarnas information fortsatte teamets efterforskningar. Frågan har de senaste åren varit vilken information en tår kan innehålla och hur mycket precision den visa.
– Nu försöker vi visa att vi kan diagnostisera Alzheimers sjukdom med samma precision som med en invasiv lumbalpunktion. Om vi kan undvika ens ett fåtal sådana ingrepp är det en framgång.
I takt med att testerna blir enklare väcks de etiska frågorna. Kommer till exempel friska människor vilja veta om deras genetiska disposition, eller kanske till och med om allvarliga sjukdomar redan börjat utvecklas.
– Det är förstås alltid bättre att genomföra ett sådant test i närvaro av en allmänläkare eller specialist. Detta gäller särskilt Alzheimers sjukdom, där botande behandling fortfarande saknas. Vill man verkligen veta? Samtidigt fick jag, när vår upptäckt uppmärksammades i medierna, många mejl från personer vars föräldrar haft demens och som själva ville veta om de bär på sjukdomen.

»Vår förhoppning är att regelbundna tårprov ska ge ny kunskap om sjukdomars förlopp och på det sätter också kunna bidra till forskningen om behandlingar.«
Etiska frågeställningar
Forskarens svar på de etiska frågorna är alltså redan utredd. Mariles Gijs är redan övertygad om att människor kommer att använda dessa tester när de blir tillgängliga. Att de har rätt att få veta.
Huntingtons sjukdom är ärftlig och debuterar oftast i vuxen ålder, men det är svårt att förutsäga exakt när. Ögonläkarens forskning riktas nu in på om det går i tårvätskan att prediktera när sjukdomen faktiskt kommer att manifestera sig.
– De allra svåraste sjukdomarna ställer förstås ändå frågor, men vi människor klarar mer än vi tror. Att veta är att kunna livsplanera. För mig som biokemist ger det störst tillfredsställelse när vi kan bidra till att förebygga eller behandla sjukdom. Vår förhoppning är att regelbundna tårprov ska ge ny kunskap om sjukdomars förlopp och på det sätter också kunna bidra till forskningen om behandlingar.
Som all banbrytande forskning har Marlies Gijs stött på motstånd. Gijs och hennes team har fullt stöd från det egna universitetet Maastricht UMC+, men infrastrukturen för det nuvarande systemet har försvarare.
– Man möter snabbt kritiker som ifrågasätter tillförlitligheten i tester baserade på tårar eller saliv. Och de representerar en mycket resursstark industri med en stark biofarmaceutisk lobby som förespråkar blodbaserade analyser, säger hon.
Universitetskliniken för oftalmologi, i samarbete med Brightlands Maastricht Health Campus, har anlitat en patentbyrå för att stödja patenteringen av fynd i tårvätska. De bedömer om resultaten är patenterbara och hjälper till att utforma och lämna in patentansökan. Därefter bistår Brightlands med att licensiera patentet eller beslutar om universitetet och forskaren själva ska kommersialisera uppfinningen och introducera testet på marknaden.
– Jag vill definitivt fortsätta vara involverad som forskare, men jag kommer inte att bli vd eller något liknande. Jag är övertygad om att tester baserade på tårforskning kommer att finnas i framtiden. Dels eftersom de erbjuder ett alternativ till invasiv provtagning, dels eftersom självtester har blivit betydligt vanligare sedan covid-19-pandemin. Acceptansen är hög. I dag vill många friska personer veta mer om sina blodvärden och vitaminnivåer. Personer med diabetes behöver redan testa sig regelbundet. Om detta kan ske utan nålstick vore det ett betydande framsteg, säger Marlies Gijs.
Det kommer dock att dröja innan det första tårbaserade testet når marknaden, bedömer Gijs. Det finns omfattande regelverk i Europa att förhålla sig till. Dessutom är kostnaderna betydande. I samarbete med University Fund Limburg, SWOL, har Gijs startat en organisation, Tear Research Network, som tidigare initierat en crowdfundingkampanj som gjorde det möjligt för organisationer och privatpersoner att direkt stödja forskning om ett innovativt diagnostiskt verktyg för Alzheimers sjukdom baserat på tårvätska.
Några av Marlies Gijs publikationer:
Association of tear fluid amyloid and tau levels with disease severity and neurodegeneration. Scientific Reports, 11(1), Article 22675. 2021
https://doi.org/10.1038/s41598-021-01993-x
High Levels of Mutant Huntingtin Protein in Tear Fluid From Huntington’s Disease Gene Expansion Carriers, Marlies Gijs et al. 2024
https://www.nature.com/articles/s41598-021-01993-x
https://www.researchgate.net/publication/
 I detta nummer möter vi oftalmologen Marlies Gijs, som visar hur tårvätska kan bära biomarkörer för sjukdomar som Parkinsons, Alzheimers och Huntingtons sjukdom. Forskningen pekar mot enklare och mer skonsamma metoder än dagens mer invasiva undersökningar, något som kan förändra framtidens diagnostik.
I detta nummer möter vi oftalmologen Marlies Gijs, som visar hur tårvätska kan bära biomarkörer för sjukdomar som Parkinsons, Alzheimers och Huntingtons sjukdom. Forskningen pekar mot enklare och mer skonsamma metoder än dagens mer invasiva undersökningar, något som kan förändra framtidens diagnostik.





